คุณสมบัติทางเคมี. การเกิดปฏิกิริยาของเบนซีนคล้ายคลึงกัน คุณสมบัติทางเคมีของเบนซีน
ปฏิกิริยากลุ่มแรกคือปฏิกิริยาการแทนที่ เรากล่าวว่า arenes ไม่มีพันธะหลายอันในโครงสร้างโมเลกุล แต่มีระบบคอนจูเกตที่มีอิเล็กตรอน 6 ตัว ซึ่งมีความเสถียรมากและให้ความแข็งแรงเพิ่มเติมแก่วงแหวนเบนซีน ดังนั้นในปฏิกิริยาเคมี อย่างแรกเลย การแทนที่ของอะตอมไฮโดรเจนจึงเกิดขึ้น ไม่ใช่การทำลายวงแหวนเบนซีน
เราได้พบปฏิกิริยาการแทนที่เมื่อพูดถึงอัลเคนแล้ว แต่สำหรับพวกมัน ปฏิกิริยาเหล่านี้ดำเนินไปตามกลไกที่ต่างไปจากเดิมอย่างสิ้นเชิง ในขณะที่ arenes มีลักษณะเฉพาะด้วยกลไกไอออนิกของปฏิกิริยาการแทนที่
อันดับแรกคุณสมบัติทางเคมี - ฮาโลเจน การแทนที่ของอะตอมไฮโดรเจนสำหรับอะตอมของฮาโลเจน - คลอรีนหรือโบรมีน
ปฏิกิริยาจะเกิดขึ้นเมื่อถูกความร้อนและมีส่วนร่วมของตัวเร่งปฏิกิริยาเสมอ ในกรณีของคลอรีนก็อาจเป็นอะลูมิเนียมคลอไรด์หรือเหล็กคลอไรด์สามชนิด ตัวเร่งปฏิกิริยาโพลาไรซ์โมเลกุลของฮาโลเจน ส่งผลให้เกิดการแตกพันธะเฮเทอโรไลติกและได้ไอออน
คลอไรด์ไอออนที่มีประจุบวกทำปฏิกิริยากับเบนซิน
หากเกิดปฏิกิริยากับโบรมีน เหล็กไตรโบรไมด์หรืออะลูมิเนียมโบรไมด์จะทำหน้าที่เป็นตัวเร่งปฏิกิริยา

สิ่งสำคัญคือต้องสังเกตว่าปฏิกิริยาเกิดขึ้นกับโมเลกุลโบรมีน ไม่ใช่กับน้ำโบรมีน เบนซีนไม่ทำปฏิกิริยากับน้ำโบรมีน
การเกิดฮาโลเจนของสารคล้ายคลึงกันเบนซินมีลักษณะเฉพาะของตัวเอง ในโมเลกุลโทลูอีน กลุ่มเมทิลอำนวยความสะดวกในการแทนที่ในวงแหวน การเกิดปฏิกิริยาเพิ่มขึ้น และปฏิกิริยาดำเนินไปภายใต้สภาวะที่รุนแรงกว่า นั่นคือที่อุณหภูมิห้องอยู่แล้ว

สิ่งสำคัญคือต้องสังเกตว่าการแทนที่จะเกิดขึ้นในตำแหน่งออร์โธและพาราเสมอ ดังนั้นจึงได้ส่วนผสมของไอโซเมอร์
ที่สองคุณสมบัติ - ไนเตรตของเบนซินการแนะนำกลุ่มไนโตรลงในวงแหวนเบนซิน

ของเหลวสีเหลืองหนักที่มีกลิ่นอัลมอนด์ขมก่อตัวขึ้น - ไนโตรเบนซีนดังนั้นปฏิกิริยานี้จึงเป็นคุณภาพของน้ำมันเบนซิน สำหรับไนเตรตจะใช้ส่วนผสมไนเตรตของกรดไนตริกและกรดซัลฟิวริกเข้มข้น ปฏิกิริยาจะดำเนินการโดยความร้อน
ให้ฉันเตือนคุณว่าสำหรับไนเตรตของอัลเคนในปฏิกิริยา Konovalov กรดไนตริกเจือจางถูกใช้โดยไม่ต้องเติมกรดซัลฟิวริก
ในไนเตรตของโทลูอีน เช่นเดียวกับในฮาโลเจน จะเกิดส่วนผสมของออร์โธ-และพารา-ไอโซเมอร์

ที่สามคุณสมบัติ - อัลคิเลชั่นของเบนซีนกับฮาโลอัลเคน

ปฏิกิริยานี้ยอมให้มีการนำไฮโดรคาร์บอนเรดิคัลเข้าไปในวงแหวนเบนซีนและถือได้ว่าเป็นวิธีการเพื่อให้ได้เบนซีนที่คล้ายคลึงกัน อะลูมิเนียมคลอไรด์ถูกใช้เป็นตัวเร่งปฏิกิริยาซึ่งส่งเสริมการสลายตัวของโมเลกุลฮาโลอัลเคนให้เป็นไอออน นอกจากนี้ยังต้องการความร้อน
ที่สี่คุณสมบัติ - alkylation ของเบนซินกับอัลคีน
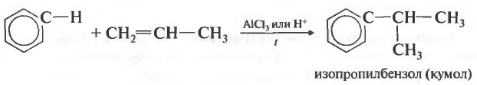
ด้วยวิธีนี้ ตัวอย่างเช่น สามารถรับคิวมีนหรือเอทิลเบนซีนได้ ตัวเร่งปฏิกิริยาคืออะลูมิเนียมคลอไรด์
2. ปฏิกิริยาการเติมเบนซิน
ปฏิกิริยากลุ่มที่สองคือปฏิกิริยาบวก เรากล่าวว่าปฏิกิริยาเหล่านี้ไม่ใช่ลักษณะเฉพาะ แต่เกิดขึ้นได้ภายใต้สภาวะที่ค่อนข้างรุนแรงด้วยการทำลายเมฆ pi-electron และการเกิดพันธะซิกมา 6 พันธะ
ที่ห้าคุณสมบัติในรายการทั่วไป - ไฮโดรจิเนชัน, การเติมไฮโดรเจน
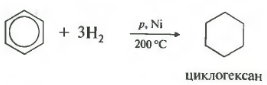
อุณหภูมิ ความดัน ตัวเร่งปฏิกิริยานิกเกิลหรือแพลตตินั่ม โทลูอีนสามารถตอบสนองในลักษณะเดียวกัน
ที่หกคุณสมบัติ - คลอรีน โปรดทราบว่าเรากำลังพูดถึงปฏิกิริยากับคลอรีนโดยเฉพาะ เนื่องจากโบรมีนไม่ทำปฏิกิริยานี้

ปฏิกิริยาเกิดขึ้นภายใต้การฉายรังสีอัลตราไวโอเลตอย่างหนัก เฮกซาคลอโรไซโคลเฮกเซน เป็นอีกชื่อหนึ่งของเฮกซาคลอเรน ก่อตัวเป็นของแข็ง
สิ่งสำคัญคือต้องจำไว้ว่าสำหรับเบนซิน เป็นไปไม่ได้ปฏิกิริยาการเติมไฮโดรเจนเฮไลด์ (ไฮโดรฮาโลจิเนชัน) และการเติมน้ำ (ไฮเดรชั่น)
3. การแทนที่ในห่วงโซ่ด้านข้างของ homologues เบนซิน
ปฏิกิริยากลุ่มที่สามเกี่ยวข้องกับความคล้ายคลึงกันของเบนซินเท่านั้น - นี่คือการแทนที่ในห่วงโซ่ด้านข้าง
ที่เจ็ดคุณสมบัติในรายการทั่วไปคือฮาโลเจนที่อะตอมอัลฟาคาร์บอนในสายด้านข้าง
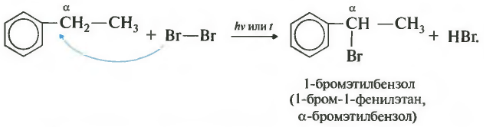
ปฏิกิริยาจะเกิดขึ้นเมื่อถูกความร้อนหรือถูกฉายรังสี และมักจะเกิดขึ้นที่อัลฟาคาร์บอนเท่านั้น ในขณะที่ฮาโลเจนดำเนินต่อไป อะตอมของฮาโลเจนที่สองจะกลับสู่ตำแหน่งอัลฟา
4. การเกิดออกซิเดชันของสารคล้ายคลึงกันเบนซิน
ปฏิกิริยากลุ่มที่สี่คือการเกิดออกซิเดชัน
แหวนเบนซินแรงเกินไปดังนั้นเบนซิน ไม่ออกซิไดซ์โพแทสเซียมเปอร์แมงกาเนต - ไม่เปลี่ยนสีของสารละลาย นี่เป็นสิ่งสำคัญมากที่ต้องจำ
ในทางกลับกัน homologues ของเบนซีนจะถูกออกซิไดซ์ด้วยสารละลายโพแทสเซียมเปอร์แมงกาเนตที่เป็นกรดเมื่อถูกความร้อน และนี่คือคุณสมบัติทางเคมีที่แปด

ปรากฎว่ากรดเบนโซอิก มีการสังเกตการเปลี่ยนสีของสารละลาย ในกรณีนี้ ไม่ว่าสายโซ่คาร์บอนของหมู่แทนที่จะยาวแค่ไหน มันก็แตกสลายหลังจากอะตอมของคาร์บอนแรกเสมอ และอะตอมอัลฟ่าจะถูกออกซิไดซ์เป็นหมู่คาร์บอกซิลด้วยการก่อตัวของกรดเบนโซอิก โมเลกุลที่เหลือจะถูกออกซิไดซ์เป็นกรดที่สอดคล้องกันหรือถ้าเป็นอะตอมของคาร์บอนเพียงอะตอมเดียวก็จะเป็นคาร์บอนไดออกไซด์
หากคล้ายคลึงกันของเบนซีนมีสารแทนที่ไฮโดรคาร์บอนมากกว่าหนึ่งตัวบนวงแหวนอะโรมาติก การเกิดออกซิเดชันจะเกิดขึ้นตามกฎเดียวกัน - คาร์บอนในตำแหน่งอัลฟ่าจะถูกออกซิไดซ์

ในตัวอย่างนี้ จะได้กรดอะโรมาติกไดบาซิก ซึ่งเรียกว่ากรดพาทาลิก
ด้วยวิธีพิเศษ ฉันสังเกตการเกิดออกซิเดชันของคิวมีน ไอโซโพรพิลเบนซีนด้วยออกซิเจนในบรรยากาศต่อหน้ากรดซัลฟิวริก

นี่เป็นวิธีที่เรียกว่าคิวมีนในการผลิตฟีนอล ตามกฎแล้วเราต้องจัดการกับปฏิกิริยานี้ในเรื่องที่เกี่ยวข้องกับการผลิตฟีนอล นี่คือวิถีทางอุตสาหกรรม
เก้าคุณสมบัติ - การเผาไหม้, ออกซิเดชันสมบูรณ์ด้วยออกซิเจน น้ำมันเบนซินและสารคล้ายคลึงกันเผาไหม้เป็นคาร์บอนไดออกไซด์และน้ำ
ให้เราเขียนสมการการเผาไหม้เบนซินในรูปแบบทั่วไป
ตามกฎการอนุรักษ์มวล ควรมีอะตอมทางด้านซ้ายมากที่สุดเท่าที่มีอะตอมทางด้านขวา เพราะในปฏิกิริยาเคมี อะตอมไม่ได้ไปไหน แต่ลำดับของพันธะระหว่างพวกมันก็เปลี่ยนไป ดังนั้นจะมีโมเลกุลของคาร์บอนไดออกไซด์มากพอๆ กับที่มีอะตอมของคาร์บอนในโมเลกุลของอารีน เนื่องจากโมเลกุลนั้นมีอะตอมของคาร์บอนอยู่หนึ่งอะตอม นั่นคือโมเลกุล n CO 2 จะมีโมเลกุลของน้ำครึ่งหนึ่งเท่ากับอะตอมไฮโดรเจน นั่นคือ (2n-6) / 2 ซึ่งหมายถึง n-3
มีจำนวนอะตอมออกซิเจนเท่ากันทางด้านซ้ายและด้านขวา ทางด้านขวามีคาร์บอนไดออกไซด์อยู่ 2n เนื่องจากมีออกซิเจน 2 อะตอมในแต่ละโมเลกุล บวกกับ n-3 จากน้ำ รวมเป็น 3n-3 ทางด้านซ้ายมีอะตอมออกซิเจนจำนวนเท่ากัน - 3n-3 ซึ่งหมายความว่ามีโมเลกุลจำนวนครึ่งหนึ่งเนื่องจากโมเลกุลประกอบด้วยอะตอมสองอะตอม นั่นคือ (3n-3)/2 โมเลกุลออกซิเจน
ดังนั้นเราจึงได้รวบรวมสมการการเผาไหม้ของสารคล้ายคลึงเบนซีนในรูปแบบทั่วไป
คำนิยาม
เบนซิน(cyclohexatriene - 1,3,5) - สารอินทรีย์ซึ่งเป็นตัวแทนที่ง่ายที่สุดของอะโรมาติกไฮโดรคาร์บอนจำนวนหนึ่ง
สูตร - C 6 H 6 (สูตรโครงสร้าง - รูปที่ 1) น้ำหนักโมเลกุล - 78, 11
ข้าว. 1. สูตรโครงสร้างและเชิงพื้นที่ของน้ำมันเบนซิน
อะตอมของคาร์บอนทั้งหกตัวในโมเลกุลเบนซีนอยู่ในสถานะไฮบริด sp 2 อะตอมของคาร์บอนแต่ละอะตอมสร้างพันธะ3σกับอะตอมของคาร์บอนอีกสองอะตอมและอะตอมไฮโดรเจนหนึ่งอะตอมที่อยู่ในระนาบเดียวกัน อะตอมของคาร์บอนหกตัวสร้างรูปหกเหลี่ยมปกติ (σ-โครงกระดูกของโมเลกุลเบนซีน) อะตอมของคาร์บอนแต่ละอะตอมมี p-orbital ที่ไม่ผสมพันธุ์หนึ่งตัวซึ่งมีอิเล็กตรอนหนึ่งตัว อิเล็กตรอน p หกตัวสร้างเมฆ π-อิเล็กตรอน (ระบบอะโรมาติก) ก้อนเดียว ซึ่งแสดงเป็นวงกลมภายในวัฏจักรที่มีสมาชิกหกตัว ไฮโดรคาร์บอนเรดิคัลที่ได้จากน้ำมันเบนซินเรียกว่า C 6 H 5 - - phenyl (Ph-)
คุณสมบัติทางเคมีของเบนซิน
เบนซีนมีลักษณะเฉพาะโดยปฏิกิริยาการทดแทนที่ดำเนินการตามกลไกอิเล็กโตรฟิลลิก:
- ฮาโลเจน (เบนซินทำปฏิกิริยากับคลอรีนและโบรมีนต่อหน้าตัวเร่งปฏิกิริยา - ปราศจาก AlCl 3, FeCl 3, AlBr 3)
C 6 H 6 + Cl 2 \u003d C 6 H 5 -Cl + HCl;
- ไนเตรต (เบนซินทำปฏิกิริยากับส่วนผสมของไนเตรตได้ง่าย - ส่วนผสมของกรดไนตริกเข้มข้นและกรดซัลฟิวริก)

- alkylation กับ alkenes
C 6 H 6 + CH 2 \u003d CH-CH 3 → C 6 H 5 -CH (CH 3) 2;
ปฏิกิริยาเพิ่มเติมกับน้ำมันเบนซินทำให้เกิดการทำลายระบบอะโรมาติกและดำเนินการภายใต้สภาวะที่ไม่เอื้ออำนวยเท่านั้น:
- ไฮโดรจิเนชัน (ปฏิกิริยาจะเกิดขึ้นเมื่อถูกความร้อน ตัวเร่งปฏิกิริยาคือ Pt)

- การเติมคลอรีน (เกิดขึ้นภายใต้การกระทำของรังสียูวีด้วยการก่อตัวของผลิตภัณฑ์ที่เป็นของแข็ง - hexachlorocyclohexane (hexachlorane) - C 6 H 6 Cl 6)

เช่นเดียวกับสารประกอบอินทรีย์อื่น ๆ น้ำมันเบนซินเข้าสู่ปฏิกิริยาการเผาไหม้ด้วยการก่อตัวของก๊าซคาร์บอนไดออกไซด์และน้ำเป็นผลิตภัณฑ์จากปฏิกิริยา (เผาไหม้ด้วยเปลวไฟที่มีควัน):
2C 6 H 6 + 15O 2 → 12CO 2 + 6H 2 O.
คุณสมบัติทางกายภาพของน้ำมันเบนซิน
เบนซินเป็นของเหลวไม่มีสี แต่มีกลิ่นฉุนเฉพาะ สร้างส่วนผสมอะซีโอทรอปิกกับน้ำ ผสมกับอีเทอร์ น้ำมันเบนซิน และตัวทำละลายอินทรีย์ต่างๆ ได้ดี จุดเดือด - 80.1C จุดหลอมเหลว - 5.5C เป็นพิษ สารก่อมะเร็ง (เช่น ก่อให้เกิดการพัฒนาของมะเร็ง)
การรับและการใช้น้ำมันเบนซิน
วิธีการหลักในการรับน้ำมันเบนซิน:
— dehydrocyclization ของเฮกเซน (ตัวเร่งปฏิกิริยา - Pt, Cr 3 O 2)
CH 3 -(CH 2) 4 -CH 3 → C 6 H 6 + 4H 2;
- ดีไฮโดรจีเนชันของไซโคลเฮกเซน (ปฏิกิริยาจะเกิดขึ้นเมื่อถูกความร้อน ตัวเร่งปฏิกิริยาคือ Pt)
C 6 H 12 → C 6 H 6 + 4H 2;
– trimerization ของอะเซทิลีน (ปฏิกิริยาจะเกิดขึ้นเมื่อถูกความร้อนถึง 600C ตัวเร่งปฏิกิริยาคือถ่านกัมมันต์)
3HC≡CH → C 6 H 6 .
เบนซีนทำหน้าที่เป็นวัตถุดิบในการผลิตสารคล้ายคลึงกัน (เอทิลเบนซีน คิวมีน) ไซโคลเฮกเซน ไนโตรเบนซีน คลอโรเบนซีน และสารอื่นๆ ก่อนหน้านี้ น้ำมันเบนซินถูกใช้เป็นสารเติมแต่งในน้ำมันเบนซินเพื่อเพิ่มค่าออกเทน แต่ตอนนี้ เนื่องจากมีความเป็นพิษสูง ปริมาณของน้ำมันเบนซินในเชื้อเพลิงจึงถูกควบคุมอย่างเข้มงวด บางครั้งใช้น้ำมันเบนซินเป็นตัวทำละลาย
ตัวอย่างการแก้ปัญหา
ตัวอย่าง 1
| ออกกำลังกาย | เขียนสมการที่คุณสามารถทำการแปลงต่อไปนี้: CH 4 → C 2 H 2 → C 6 H 6 → C 6 H 5 Cl |
| การตัดสินใจ | เพื่อให้ได้อะเซทิลีนจากมีเทนจะใช้ปฏิกิริยาต่อไปนี้: 2CH 4 → C 2 H 2 + 3H 2 (t = 1400C) การรับน้ำมันเบนซินจากอะเซทิลีนเป็นไปได้โดยปฏิกิริยาของ trimerization ของอะเซทิลีนซึ่งเกิดขึ้นเมื่อถูกความร้อน (t = 600C) และต่อหน้าถ่านกัมมันต์: 3C 2 H 2 → C 6 H 6 . ปฏิกิริยาคลอรีนของเบนซินเพื่อให้ได้คลอโรเบนซีนเป็นผลิตภัณฑ์จะดำเนินการต่อหน้าเหล็ก (III) คลอไรด์: C 6 H 6 + Cl 2 → C 6 H 5 Cl + HCl |
ตัวอย่าง 2
| ออกกำลังกาย | เติมน้ำมันเบนซิน 39 กรัมต่อหน้าเหล็ก (III) คลอไรด์ 1 โมลของน้ำโบรมีน ปริมาณของสารคืออะไรและได้ผลลัพธ์เป็นผลิตภัณฑ์กี่กรัม? |
| การตัดสินใจ | ให้เราเขียนสมการสำหรับปฏิกิริยาของโบรมีนเบนซีนต่อหน้าเหล็ก (III) คลอไรด์: C 6 H 6 + Br 2 → C 6 H 5 Br + HBr. ผลิตภัณฑ์จากปฏิกิริยา ได้แก่ โบรโมเบนซีนและไฮโดรเจนโบรไมด์ มวลโมเลกุลของน้ำมันเบนซิน คำนวณโดยใช้ตารางองค์ประกอบทางเคมีของ D.I. เมนเดเลเยฟ - 78 ก./โมล หาปริมาณสารเบนซีน: n(C 6 H 6) = m(C 6 H 6) / M(C 6 H 6); n(C 6 H 6) = 39/78 = 0.5 โมล ตามสภาพของปัญหา เบนซินทำปฏิกิริยากับโบรมีน 1 โมล ดังนั้นน้ำมันเบนซินจึงขาดตลาดและจะทำการคำนวณเพิ่มเติมสำหรับน้ำมันเบนซิน ตามสมการปฏิกิริยา n (C 6 H 6): n (C 6 H 5 Br) : n (HBr) \u003d 1: 1: 1 ดังนั้น n (C 6 H 6) \u003d n (C 6 H 5 Br) \u003d: n(HBr) = 0.5 โมล จากนั้นมวลของโบรโมเบนซีนและไฮโดรเจนโบรไมด์จะเท่ากัน: m(C 6 H 5 Br) = n(C 6 H 5 Br)×M(C 6 H 5 Br); m(HBr) = n(HBr)×M(HBr) มวลโมลาร์ของโบรโมเบนซีนและไฮโดรเจนโบรไมด์ คำนวณโดยใช้ตารางองค์ประกอบทางเคมีของ D.I. Mendeleev - 157 และ 81 g/mol ตามลำดับ ม.(C 6 H 5 Br) = 0.5×157 = 78.5 กรัม; ม.(HBr) = 0.5 x 81 = 40.5 กรัม |
| ตอบ | ผลิตภัณฑ์จากปฏิกิริยา ได้แก่ โบรโมเบนซีนและไฮโดรเจนโบรไมด์ มวลของโบรโมเบนซีนและไฮโดรเจนโบรไมด์คือ 78.5 และ 40.5 กรัมตามลำดับ |
สารประกอบเช่นเบนซินนางเคมีในบ้านของเธอในที่สุดและได้มาโดยไม่สามารถเพิกถอนได้ในปี พ.ศ. 2376 เท่านั้น เบนซินเป็นสารประกอบที่มีอารมณ์ฉุนเฉียว บางคนอาจพูดได้ แม้กระทั่งลักษณะระเบิด คุณรู้ได้อย่างไร?
เรื่องราว
Johann Glauber ในปี 1649 หันความสนใจไปที่สารประกอบที่ก่อตัวขึ้นได้สำเร็จในขณะที่นักเคมีกำลังทำงานเกี่ยวกับน้ำมันดิน แต่มันต้องการที่จะไม่ระบุตัวตน
หลังจากผ่านไปประมาณ 170 ปีและเพื่อให้แม่นยำยิ่งขึ้นในช่วงกลางทศวรรษที่ยี่สิบของศตวรรษที่ XIX โดยบังเอิญ น้ำมันเบนซินถูกสกัดจากก๊าซแสงสว่าง กล่าวคือจากคอนเดนเสทที่ปล่อยออกมา มนุษยชาติเป็นหนี้ความพยายามดังกล่าวต่อ Michael Faraday นักวิทยาศาสตร์จากอังกฤษ
กระบองสำหรับการซื้อน้ำมันเบนซินถูกสกัดกั้นโดย Eilgard Mitscherlich ชาวเยอรมัน สิ่งนี้เกิดขึ้นระหว่างการประมวลผลเกลือแคลเซียมแอนไฮดรัสของกรดเบนโซอิก บางทีนั่นอาจเป็นเหตุผลว่าทำไมสารประกอบจึงได้รับชื่อดังกล่าว - เบนซิน นักวิทยาศาสตร์เรียกมันว่าน้ำมันเบนซินเป็นตัวเลือกหนึ่ง ธูปถ้าแปลจากภาษาอาหรับ
น้ำมันเบนซินเผาไหม้อย่างสวยงามและสว่างสดใส จากการสังเกตเหล่านี้ ออกุสต์ โลร็องต์ แนะนำให้เรียกมันว่า "เฟน" หรือ "เบนซีน" สว่างไสว - ถ้าแปลจากภาษากรีก
จากความคิดเห็นของแนวคิดเกี่ยวกับธรรมชาติของพันธะอิเล็กทรอนิกส์ คุณสมบัติของน้ำมันเบนซิน นักวิทยาศาสตร์ได้จัดเตรียมโมเลกุลของสารประกอบไว้ในรูปแบบของภาพต่อไปนี้ นี่คือรูปหกเหลี่ยม วงกลมถูกจารึกไว้ในนั้น สิ่งที่กล่าวมาข้างต้นชี้ให้เห็นว่าน้ำมันเบนซินมีเมฆอิเล็กตรอนรวมอยู่ด้วย ซึ่งมีอะตอมของคาร์บอนในวัฏจักรหก (โดยไม่มีข้อยกเว้น) อย่างปลอดภัย ไม่มีพันธะไบนารีคงที่
ก่อนหน้านี้เบนซีนเคยเป็นตัวทำละลาย แต่โดยพื้นฐานแล้ว อย่างที่พวกเขาพูด เขาไม่ได้เป็นสมาชิก ไม่เข้าร่วม ไม่เกี่ยวข้อง แต่นี่อยู่ในศตวรรษที่ 19 การเปลี่ยนแปลงที่สำคัญเกิดขึ้นใน XX คุณสมบัติของน้ำมันเบนซินแสดงถึงคุณสมบัติที่มีค่าที่สุดที่ช่วยให้เขาได้รับความนิยมมากขึ้น ค่าออกเทนที่สูงทำให้สามารถใช้เป็นเชื้อเพลิงในการเติมเชื้อเพลิงรถยนต์ได้ การกระทำนี้เป็นแรงผลักดันให้มีการถอนเบนซีนออกไปอย่างกว้างขวาง ซึ่งการสกัดจะดำเนินการเป็นผลพลอยได้จากการโค้กของการผลิตเหล็ก
ในวัยสี่สิบ ในด้านเคมี น้ำมันเบนซินเริ่มถูกใช้ในการผลิตสารที่ระเบิดอย่างรวดเร็ว ศตวรรษที่ 20 ครองตำแหน่งตัวเองด้วยข้อเท็จจริงที่ว่าอุตสาหกรรมการกลั่นน้ำมันผลิตน้ำมันเบนซินได้มากจนเริ่มจัดหาอุตสาหกรรมเคมี
ลักษณะของน้ำมันเบนซิน
ไฮโดรคาร์บอนไม่อิ่มตัวนั้นคล้ายกับเบนซินมาก ตัวอย่างเช่น ชุดไฮโดรคาร์บอนของเอทิลีนแสดงคุณลักษณะของตัวเองว่าเป็นไฮโดรคาร์บอนที่ไม่อิ่มตัว มันมีปฏิกิริยาบวก เบนซินเต็มใจเข้าสู่ ทั้งหมดนี้ต้องขอบคุณอะตอมที่อยู่ในระนาบเดียวกัน และตามความเป็นจริงแล้ว เมฆอิเล็กตรอนแบบคอนจูเกต

หากมีวงแหวนเบนซีนอยู่ในสูตร เราก็สามารถสรุปเบื้องต้นได้ว่านี่คือเบนซีน ซึ่งมีสูตรโครงสร้างออกมาประมาณนี้
คุณสมบัติทางกายภาพ
เบนซินเป็นของเหลวไม่มีสี แต่มีกลิ่นอับ น้ำมันเบนซินละลายเมื่ออุณหภูมิสูงถึง 5.52 องศาเซลเซียส เดือดที่ 80.1 ความหนาแน่น 0.879 g / cm 3 มวลโมลาร์คือ 78.11 g / mol เมื่อเผาไหม้จะเกิดควันมาก เกิดสารประกอบระเบิดเมื่ออากาศเข้าไป หิน (น้ำมันเบนซิน อีเธอร์และอื่น ๆ ) ถูกรวมเข้ากับสารที่อธิบายไว้โดยไม่มีปัญหา สารประกอบ azeotropic สร้างขึ้นด้วยน้ำ การให้ความร้อนก่อนการกลายเป็นไอจะเกิดขึ้นที่ 69.25 องศา (เบนซิน 91%) ที่อุณหภูมิ 25 องศาเซลเซียส สามารถละลายน้ำได้ 1.79 กรัม/ลิตร
คุณสมบัติทางเคมี
เบนซีนทำปฏิกิริยากับกรดซัลฟิวริกและกรดไนตริก และยังมีแอลคีน ฮาโลเจน คลอโรอัลเคน ปฏิกิริยาการทดแทนคือสิ่งที่เป็นลักษณะเฉพาะของเขา อุณหภูมิแรงดันส่งผลต่อการทะลุทะลวงของวงแหวนเบนซิน ซึ่งเกิดขึ้นภายใต้สภาวะที่ค่อนข้างรุนแรง
เราสามารถพิจารณาแต่ละสมการปฏิกิริยาเบนซีนโดยละเอียดยิ่งขึ้น
1. การทดแทนด้วยไฟฟ้า โบรมีนต่อหน้าตัวเร่งปฏิกิริยาจะทำปฏิกิริยากับคลอรีน ผลลัพธ์คือคลอโรเบนซีน:
С6H6+3Cl2 → C6H5Cl + HCl
2. ปฏิกิริยาของ Friedel-Crafts หรือ benzene alkylation การปรากฏตัวของอัลคิลเบนซีนเกิดขึ้นเนื่องจากการรวมกันกับอัลเคนซึ่งเป็นอนุพันธ์ของฮาโลเจน:
C6H6 + C2H5Br → C6H5C2H5 + HBr
3. การทดแทนด้วยไฟฟ้า นี่คือปฏิกิริยาของไนเตรตและซัลโฟเนชัน สมการเบนซินจะมีลักษณะดังนี้:
C6H6 + H2SO4 → C6H5SO3H + H2O
C6H6 + HNO3 → C6H5NO2 + H2O
4. น้ำมันเบนซินเมื่อเผาไหม้:
2C6H6 + 15O2 → 12CO2 + 6H2O
ภายใต้เงื่อนไขบางประการ มันแสดงลักษณะเฉพาะของไฮโดรคาร์บอนอิ่มตัว p-electron cloud ซึ่งอยู่ในโครงสร้างของสารที่อยู่ระหว่างการพิจารณา อธิบายปฏิกิริยาเหล่านี้
เบนซินประเภทต่างๆ ขึ้นอยู่กับเทคโนโลยีพิเศษ นี่คือที่มาของการติดฉลากน้ำมันเบนซิน ตัวอย่างเช่น การทำให้บริสุทธิ์และการทำให้บริสุทธิ์ที่สูงขึ้นสำหรับการสังเคราะห์ ฉันต้องการจะแยกสังเกตคุณสมบัติทางเคมีของน้ำมันเบนซินที่คล้ายคลึงกันและเฉพาะเจาะจงมากขึ้น เหล่านี้คืออัลคิลเบนซีน

homologues ของเบนซีนมีแนวโน้มที่จะตอบสนองมากขึ้น แต่ปฏิกิริยาข้างต้นของเบนซีน กล่าวคือ คล้ายคลึงกัน เกิดขึ้นด้วยความแตกต่างบางประการ
ฮาโลเจนของอัลคิลเบนซีน
รูปแบบของสมการจะเป็นดังนี้:
С6H5-CH3 + Br = C6H5-CH2Br + HBr
ไม่พบความทะเยอทะยานของโบรมีนในวงแหวนเบนซิน มันเข้าไปในห่วงโซ่ที่ด้านข้าง แต่ต้องขอบคุณตัวเร่งปฏิกิริยาเกลือ Al(+3) โบรมีนจึงเข้าสู่วงแหวนอย่างกล้าหาญ
ไนเตรตของอัลคิลเบนซีน
ต้องขอบคุณกรดกำมะถันและไนตริก เบนซีนและอัลคิลเบนซีนจึงถูกไนเตรท ปฏิกิริยาอัลคิลเบนซีน ได้ผลิตภัณฑ์สองชิ้นจากการนำเสนอสามรายการ - เหล่านี้เป็นพารา- และออร์โธ-ไอโซเมอร์ คุณสามารถเขียนหนึ่งในสูตร:
C6H5 - CH3 + 3HNO3 → C6H2CH3 (NO2)3.
ออกซิเดชัน
สำหรับน้ำมันเบนซินนี่เป็นสิ่งที่ยอมรับไม่ได้ แต่อัลคิลเบนซีนตอบสนองด้วยความเต็มใจ เช่น กรดเบนโซอิก สูตรอยู่ด้านล่าง:
C6H5CH3 + [O] → C6H5COOH
แอลคิลเบนซีนและเบนซีน ไฮโดรจิเนชันของพวกมัน
ในที่ที่มีสารเอนแฮนเซอร์ ไฮโดรเจนเริ่มทำปฏิกิริยากับเบนซีน ส่งผลให้เกิดการก่อตัวของไซโคลเฮกเซนตามที่กล่าวไว้ข้างต้น ในทำนองเดียวกัน อัลคิลเบนซีนจะถูกแปลงเป็นอัลคิลไซโคลเฮกเซนได้ง่าย เพื่อให้ได้อัลคิลไซโคลเฮกเซน จำเป็นต้องให้อัลคิลเบนซีนที่ต้องการไฮโดรจิเนชัน โดยทั่วไป เป็นขั้นตอนที่จำเป็นสำหรับการผลิตผลิตภัณฑ์บริสุทธิ์ และนี่ไม่ใช่ปฏิกิริยาทั้งหมดของเบนซินและอัลคิลเบนซีน
การผลิตน้ำมันเบนซิน อุตสาหกรรม
รากฐานของการผลิตดังกล่าวขึ้นอยู่กับการแปรรูปส่วนประกอบ ได้แก่ โทลูอีน แนฟทา ทาร์ ซึ่งถูกปล่อยออกมาระหว่างการแตกร้าวของถ่านหิน และอื่นๆ ดังนั้นน้ำมันเบนซินจึงถูกผลิตขึ้นในสถานประกอบการปิโตรเคมีและโลหการ สิ่งสำคัญคือต้องรู้วิธีรับน้ำมันเบนซินที่มีระดับการทำให้บริสุทธิ์ที่แตกต่างกัน เนื่องจากแบรนด์ของสารนี้ขึ้นอยู่กับหลักการผลิตและวัตถุประสงค์โดยตรง
ส่วนแบ่งของสิงโตทำโดยการปฏิรูปเทอร์โมแคตาไลติกของส่วน caustobiolite โดยเดือดที่ 65 องศาโดยมีผลของสารสกัดการกลั่นด้วยไดเมทิลฟอร์มาไมด์
ในระหว่างการผลิตเอทิลีนและโพรพิลีนจะได้ผลิตภัณฑ์ที่เป็นของเหลวซึ่งเกิดขึ้นระหว่างการสลายตัวของสารประกอบอนินทรีย์และอินทรีย์ภายใต้อิทธิพลของความร้อน ในจำนวนนี้น้ำมันเบนซินถูกแยกออก แต่น่าเสียดายที่ไม่มีแหล่งข้อมูลสำหรับตัวเลือกการผลิตเบนซินนี้มากนัก ดังนั้น เนื้อหาที่เราสนใจจึงถูกผลิตขึ้นโดยการปฏิรูป โดยวิธีนี้จะทำให้ปริมาณน้ำมันเบนซินเพิ่มขึ้น

โดยการจัดการที่อุณหภูมิ 610-830 องศาพร้อมเครื่องหมายบวก เมื่อมีไอน้ำเกิดขึ้นระหว่างการต้มน้ำและไฮโดรเจน เบนซีนจะได้รับจากโทลูอีน มีตัวเลือกอื่น - ตัวเร่งปฏิกิริยา เมื่อสังเกตเห็นการปรากฏตัวของซีโอไลต์หรือตัวเร่งปฏิกิริยาออกไซด์อีกทางหนึ่งภายใต้ระบอบอุณหภูมิ 227-627 องศา
มีอีกวิธีหนึ่งที่เก่ากว่าในการพัฒนาน้ำมันเบนซิน ด้วยความช่วยเหลือของการดูดซึมโดยตัวดูดซับอินทรีย์ มันถูกแยกออกจากผลสุดท้ายของถ่านโค้ก ผลิตภัณฑ์นี้เป็นก๊าซไอน้ำและผ่านการทำความเย็นล่วงหน้าแล้ว ตัวอย่างเช่น น้ำมันถูกใช้ซึ่งแหล่งที่มาของน้ำมันหรือถ่านหิน เมื่อกลั่นด้วยไอน้ำ คนเก็บขยะจะถูกแยกออก Hydrotreating ช่วยขจัดน้ำมันเบนซินดิบจากสารส่วนเกิน
วัตถุดิบถ่านหิน
ในทางโลหะวิทยา เมื่อใช้ถ่านหินหรือให้ละเอียดยิ่งขึ้น ได้โค้กจากการกลั่นแบบแห้ง ในระหว่างขั้นตอนนี้ การจ่ายอากาศจะถูกจำกัด อย่าลืมว่าถ่านหินถูกทำให้ร้อนที่อุณหภูมิ 1200-1500 องศาเซลเซียส
น้ำมันเบนซินเคมีถ่านหินต้องการการทำให้บริสุทธิ์อย่างละเอียด จำเป็นต้องกำจัดเมทิลไซโคลเฮกเซนและเอ็นเฮปเทนสหายของมันโดยไม่ล้มเหลว ควรถอดออกด้วย น้ำมันเบนซินจะต้องผ่านกระบวนการคัดแยก การทำให้บริสุทธิ์ ซึ่งจะดำเนินการมากกว่าหนึ่งครั้ง
วิธีการที่อธิบายไว้ข้างต้นเป็นวิธีที่เก่าแก่ที่สุด แต่เมื่อเวลาผ่านไปก็จะสูญเสียตำแหน่งที่สูง
เศษส่วนของน้ำมัน
0.3-1.2% - ตัวบ่งชี้ดังกล่าวขององค์ประกอบของฮีโร่ของเราในน้ำมันดิบ ตัวบ่งชี้ที่ไม่เพียงพอในการลงทุนด้านการเงินและกองกำลัง เป็นการดีที่สุดที่จะใช้ขั้นตอนทางอุตสาหกรรมสำหรับการประมวลผลเศษส่วนของปิโตรเลียม นั่นคือการปฏิรูปตัวเร่งปฏิกิริยา เมื่อมีแอมพลิฟายเออร์อะลูมิเนียม - แพลตตินั่ม - รีเนียม เปอร์เซ็นต์ของการรวมคาร์โบไฮเดรตอะโรมาติกจะเพิ่มขึ้น และตัวบ่งชี้ที่กำหนดความสามารถของเชื้อเพลิงที่จะไม่จุดไฟเองตามธรรมชาติในระหว่างการอัดจะเพิ่มขึ้น
ไพโรไลซิสเรซิน
หากผลิตภัณฑ์น้ำมันของเราสกัดจากวัตถุดิบที่ไม่ใช่ของแข็ง กล่าวคือ โดยไพโรไลซิสของโพรพิลีนและเอทิลีนที่เกิดขึ้นในการผลิต แนวทางนี้จะเป็นที่ยอมรับได้มากที่สุด เพื่อให้แม่นยำยิ่งขึ้น น้ำมันเบนซินจะถูกปล่อยออกมาจากไพโรคอนเดนเสท การสลายตัวของเศษส่วนบางชนิดต้องใช้ไฮโดรทรีตเมนต์ สารผสมกำมะถันและไม่อิ่มตัวจะถูกลบออกระหว่างการทำความสะอาด ในผลลัพธ์เบื้องต้น สังเกตเนื้อหาของไซลีน โทลูอีน เบนซิน ด้วยความช่วยเหลือของการกลั่นซึ่งเป็นสารสกัด กลุ่ม BTX จะถูกแยกออกและรับเบนซีน

ไฮโดรดีอัลคิเลชันของโทลูอีน
ตัวเอกของกระบวนการ ค็อกเทลของการไหลของไฮโดรเจนและโทลูอีน ถูกป้อนความร้อนเข้าสู่เครื่องปฏิกรณ์ โทลูอีนผ่านเตียงตัวเร่งปฏิกิริยา ในระหว่างกระบวนการนี้ กลุ่มเมทิลจะถูกแยกออกเพื่อสร้างเบนซิน มีวิธีการบางอย่างของการทำให้บริสุทธิ์ที่นี่ ผลที่ได้คือสารบริสุทธิ์สูง (สำหรับไนเตรต)
ความไม่สมส่วนโทลูอีน
อันเป็นผลมาจากการปฏิเสธคลาสเมทิลทำให้เกิดเบนซีนไซลีนจะถูกออกซิไดซ์ ในกระบวนการนี้ มีการสังเกตทรานส์อัลคิเลชัน ตัวเร่งปฏิกิริยาเกิดจากแพลเลเดียม แพลตตินั่ม และนีโอไดเมียม ซึ่งอยู่บนอะลูมิเนียมออกไซด์
โทลูอีนและไฮโดรเจนถูกส่งไปยังเครื่องปฏิกรณ์ด้วยเตียงตัวเร่งปฏิกิริยาที่เสถียร จุดประสงค์คือเพื่อป้องกันไม่ให้ไฮโดรคาร์บอนตกตะกอนบนระนาบตัวเร่งปฏิกิริยา กระแสที่ออกจากเครื่องปฏิกรณ์จะถูกทำให้เย็นลง และไฮโดรเจนก็ถูกนำกลับมาใช้ใหม่ได้อย่างปลอดภัย สิ่งที่เหลืออยู่กลั่นสามครั้ง ในระยะเริ่มต้น สารประกอบที่ไม่ใช่อะโรมาติกจะถูกถอนออก น้ำมันเบนซินถูกสกัดครั้งที่สอง และขั้นตอนสุดท้ายคือการสกัดไซลีน
อะเซทิลีนไตรเมอร์
ด้วยผลงานของนักเคมีกายภาพชาวฝรั่งเศส Marcelin Berthelot ทำให้น้ำมันเบนซินเริ่มผลิตจากอะเซทิลีน แต่ในขณะเดียวกัน ค็อกเทลหนักๆ ก็โดดเด่นกว่าองค์ประกอบอื่นๆ มากมาย คำถามคือจะลดอุณหภูมิปฏิกิริยาได้อย่างไร คำตอบนั้นได้รับเมื่อสิ้นสุดอายุสี่สิบของศตวรรษที่ XX เท่านั้น V. Reppe พบตัวเร่งปฏิกิริยาที่เหมาะสม กลายเป็นนิกเกิล Trimerization เป็นวิธีเดียวที่จะได้เบนซินจากอะเซทิลีน

การก่อตัวของน้ำมันเบนซินเกิดขึ้นด้วยความช่วยเหลือของถ่านกัมมันต์ ที่อัตราความร้อนสูง อะเซทิลีนจะผ่านถ่านหิน น้ำมันเบนซินจะถูกปล่อยออกมาหากอุณหภูมิอย่างน้อย 410 องศา ในเวลาเดียวกัน อะโรมาติกไฮโดรคาร์บอนหลายชนิดยังคงถือกำเนิดขึ้น ดังนั้นจึงจำเป็นต้องมีอุปกรณ์ที่ดีที่สามารถกรองอะเซทิลีนให้บริสุทธิ์ได้ในเชิงคุณภาพ ด้วยวิธีการที่ลำบากเช่น trimerization อะเซทิลีนจำนวนมากจึงถูกใช้ไป เพื่อให้ได้น้ำมันเบนซิน 15 มล. ต้องใช้อะเซทิลีน 20 ลิตร คุณสามารถดูลักษณะของปฏิกิริยาจะใช้เวลาไม่นาน
3C2H2 → C6H6 (สมการเซลินสกี้)
3CH → CH = (t, kat) = C6H6.
น้ำมันเบนซินใช้ที่ไหน
น้ำมันเบนซินเป็นผลิตผลของเคมีที่ได้รับความนิยมอย่างมาก โดยเฉพาะอย่างยิ่งมักสังเกตว่าใช้เบนซีนในการผลิตคิวมีน, ไซโคลเฮกเซน, เอทิลเบนซีนอย่างไร ในการสร้างสไตรีนนั้น เอทิลเบนซีนเป็นสิ่งที่ขาดไม่ได้ วัสดุเริ่มต้นสำหรับการผลิตคาโปรแลคตัมคือไซโคลเฮกเซน เมื่อทำเทอร์โมพลาสติกเรซิน จะใช้คาโปรแลคตัม สารที่อธิบายไว้นี้ขาดไม่ได้ในการผลิตสีและสารเคลือบเงาต่างๆ
เบนซิน อันตรายแค่ไหน
เบนซินเป็นสารพิษ การแสดงความรู้สึกไม่สบายซึ่งมาพร้อมกับอาการคลื่นไส้และเวียนศีรษะรุนแรงเป็นสัญญาณของการเป็นพิษ แม้แต่ความตายก็ไม่เว้น ความรู้สึกของความสุขที่อธิบายไม่ได้คือเสียงระฆังที่น่ารำคาญไม่น้อยในกรณีที่เป็นพิษจากน้ำมันเบนซิน
น้ำมันเบนซินทำให้เกิดการระคายเคืองผิวหนัง ไอระเหยของน้ำมันเบนซินสามารถซึมผ่านได้ง่ายแม้ผ่านผิวหนังที่ไม่เสียหาย ด้วยการสัมผัสกับสารในระยะสั้นที่สุดในขนาดที่เล็ก แต่เป็นประจำผลที่ไม่พึงประสงค์จะไม่นาน ซึ่งอาจเป็นรอยโรคของไขกระดูกและมะเร็งเม็ดเลือดขาวชนิดเฉียบพลันได้หลายชนิด

นอกจากนี้สารเสพติดในมนุษย์ น้ำมันเบนซินทำหน้าที่เหมือนยาเสพติด ควันบุหรี่ทำให้เกิดผลิตภัณฑ์คล้ายน้ำมันดิน เมื่อพวกเขาศึกษาก็สรุปได้ว่าเนื้อหาของหลังไม่ปลอดภัยสำหรับมนุษย์ นอกจากการมีอยู่ของนิโคตินแล้ว ยังพบการมีอยู่ของคาร์โบไฮเดรตอะโรมาติกในประเภทเบนไพรีนอีกด้วย คุณสมบัติที่โดดเด่นของ benzpyrene เป็นสารก่อมะเร็ง พวกมันมีผลเสียอย่างมาก ตัวอย่างเช่น ทำให้เกิดมะเร็ง
น้ำมันเบนซินเป็นวัสดุเริ่มต้นสำหรับการผลิตยาหลายชนิด พลาสติก ยางสังเคราะห์ และแน่นอน สีย้อม นี่คือผลิตผลทางสมองที่พบบ่อยที่สุดของเคมีและสารประกอบอะโรมาติก
โครงสร้างวัฏจักรของเบนซินได้รับการเสนอครั้งแรกโดย F.A. Kekule ใน พ.ศ. 2408

Friedrich August Kekule von Stradonitz เป็นนักเคมีชาวเยอรมันที่โดดเด่นในศตวรรษที่ 19 ในปี ค.ศ. 1854 เขาค้นพบสารประกอบอินทรีย์ชนิดแรกที่มีกรดซัลเฟอร์ - ไทโออะซิติก (กรดไธโอเอทาโนอิก) นอกจากนี้ เขายังได้สร้างโครงสร้างของสารประกอบไดอาโซ อย่างไรก็ตาม ผลงานที่มีชื่อเสียงที่สุดของเขาในการพัฒนาเคมีคือการจัดตั้งโครงสร้างของน้ำมันเบนซิน (1866) Kekule แสดงให้เห็นว่าพันธะคู่ของเบนซินสลับกันรอบวงแหวน (ความคิดนี้เกิดขึ้นกับเขาครั้งแรกในความฝัน) เขาแสดงให้เห็นในภายหลังว่าการจัดเรียงพันธะคู่ที่เป็นไปได้ทั้งสองแบบเหมือนกัน และวงแหวนเบนซินเป็นไฮบริดระหว่างโครงสร้างทั้งสอง ดังนั้น เขาจึงคาดหวังแนวคิดเรื่องการสั่นพ้อง (mesomerism) ซึ่งปรากฏในทฤษฎีพันธะเคมีในช่วงต้นทศวรรษ 1930
ถ้าเบนซีนมีโครงสร้างแบบนี้จริง ๆ แล้วอนุพันธ์แทน 1,2 ตัวของมันควรมีไอโซเมอร์สองตัวแต่ละตัว ตัวอย่างเช่น,

อย่างไรก็ตาม ไม่มีเบนซีนที่ถูกแทนที่ 1,2 ชนิดใดที่สามารถแยกไอโซเมอร์สองชนิดได้
ดังนั้น Kekule จึงแนะนำว่าโมเลกุลของเบนซีนมีอยู่เป็นโครงสร้างสองโครงสร้างที่ผ่านเข้าสู่กันและกันอย่างรวดเร็ว:

โปรดทราบว่าการแสดงแผนผังดังกล่าวของโมเลกุลเบนซีนและอนุพันธ์ของพวกมันมักจะไม่ได้ระบุอะตอมของไฮโดรเจนที่ติดอยู่กับอะตอมคาร์บอนของวงแหวนเบนซีน
ในเคมีสมัยใหม่ โมเลกุลของเบนซีนถือเป็นลูกผสมที่มีจังหวะจำกัดทั้งสองรูปแบบ (ดูหัวข้อ 2.1) อีกคำอธิบายหนึ่งของโมเลกุลเบนซีนขึ้นอยู่กับการพิจารณาออร์บิทัลของโมเลกุล ในวินาที 3.1 มีการบ่งชี้ว่า -อิเล็กตรอนที่อยู่ในออร์บิทัลพันธะถูกแยกออกจากกันระหว่างอะตอมของคาร์บอนทั้งหมดของวงแหวนเบนซีนและก่อตัวเป็นเมฆอิเล็กตรอน ตามการแสดงนี้ โมเลกุลของเบนซีนสามารถอธิบายตามอัตภาพได้ดังนี้:
ข้อมูลการทดลองยืนยันการมีอยู่ของโครงสร้างดังกล่าวในน้ำมันเบนซิน ถ้าเบนซินมีโครงสร้างที่ Kekule เสนอในตอนแรก โดยมีพันธะคู่สามคอนจูเกต เบนซินจะต้องทำปฏิกิริยาเหมือนแอลคีน อย่างไรก็ตาม ตามที่กล่าวไว้ข้างต้น น้ำมันเบนซินไม่ทำปฏิกิริยาเพิ่มเติม นอกจากนี้ น้ำมันเบนซินยังมีความเสถียรมากกว่าน้ำมันที่มีพันธะคู่แบบแยกเดี่ยวสามพันธะ ในวินาที 5.3 พบว่าเอนทาลปีของไฮโดรจิเนชันของเบนซินกับการเกิดไซโคลเฮกเซนมีค่าลบมากกว่า
ตารางที่ 18.3 ความยาวของพันธะคาร์บอน-คาร์บอนต่างๆ


ข้าว. 18.6. โครงสร้างทางเรขาคณิตของโมเลกุลเบนซีน
มีค่ามากกว่าสามเท่าของเอนทาลปีของไฮโดรจิเนชันของไซโคลเฮกซีน ความแตกต่างระหว่างค่าเหล่านี้มักจะเรียกว่าเอนทาลปี delocalization พลังงานพ้อง หรือพลังงานรักษาเสถียรภาพของเบนซิน
พันธะคาร์บอน-คาร์บอนทั้งหมดในวงแหวนเบนซีนมีความยาวเท่ากัน ซึ่งน้อยกว่าความยาวของพันธะ C-C ในอัลเคน แต่ยาวกว่าความยาวของพันธะ C=C ในอัลคีน (ตารางที่ 18.3) สิ่งนี้เป็นการยืนยันว่าพันธะคาร์บอน-คาร์บอนในน้ำมันเบนซินเป็นลูกผสมระหว่างพันธะเดี่ยวและพันธะคู่
โมเลกุลเบนซีนมีโครงสร้างแบน ดังแสดงในรูปที่ 18.6.
คุณสมบัติทางกายภาพ
ภายใต้สภาวะปกติ น้ำมันเบนซินเป็นของเหลวไม่มีสีที่แข็งตัวที่ 5.5 ° C และเดือดที่ 80 ° C มีกลิ่นที่น่าพึงพอใจ แต่ดังที่ได้กล่าวไว้ข้างต้นมีความเป็นพิษสูง น้ำมันเบนซินไม่สามารถผสมกับน้ำได้ และในระบบน้ำมันเบนซิน น้ำจะสร้างชั้นบนสุดของสองชั้น อย่างไรก็ตาม สามารถละลายได้ในตัวทำละลายอินทรีย์ที่ไม่มีขั้ว และเป็นตัวทำละลายที่ดีสำหรับสารประกอบอินทรีย์อื่นๆ
คุณสมบัติทางเคมี
แม้ว่าน้ำมันเบนซินจะเข้าสู่ปฏิกิริยาการเติมบางอย่าง (ดูด้านล่าง) แต่ก็ไม่ได้แสดงปฏิกิริยาตามแบบฉบับของแอลคีนในตัวมัน ตัวอย่างเช่น จะไม่ทำให้น้ำโบรมีนหรือสารละลาย α-ion เปลี่ยนสี นอกจากนี้ เบนซิน
ทำปฏิกิริยาเพิ่มเติมกับกรดแก่ เช่น กรดไฮโดรคลอริกหรือกรดซัลฟิวริก
ในเวลาเดียวกัน น้ำมันเบนซินมีส่วนร่วมในปฏิกิริยาการแทนที่อิเล็กโทรฟิลิกจำนวนหนึ่ง สารประกอบอะโรมาติกเป็นผลผลิตจากปฏิกิริยาประเภทนี้ เนื่องจากระบบอิเลคตรอนแบบแยกส่วน - อิเล็กตรอนของเบนซีนจะคงอยู่ในปฏิกิริยาเหล่านี้ กลไกทั่วไปของการแทนที่อะตอมไฮโดรเจนบนวงแหวนเบนซีนด้วยอิเล็กโทรฟิลบางชนิดได้อธิบายไว้ในข้อ 17.3. ตัวอย่างของการทดแทนน้ำมันเบนซินด้วยไฟฟ้า ได้แก่ ปฏิกิริยาไนเตรต ฮาโลเจน ซัลโฟเนชัน และปฏิกิริยาของ Friedel-Crafts
ไนเตรท เบนซีนสามารถไนเตรตได้ (แนะนำกลุ่มเข้าไป) โดยการบำบัดด้วยส่วนผสมของกรดไนตริกเข้มข้นและกรดซัลฟิวริก:

ไนโตรเบนซีน
สภาวะสำหรับปฏิกิริยานี้และกลไกของปฏิกิริยาได้อธิบายไว้ในข้อ 17.3.
ไนโตรเบนซีนเป็นของเหลวสีเหลืองซีดมีกลิ่นอัลมอนด์ ในระหว่างการไนเตรตของเบนซีนนอกเหนือจากไนโตรเบนซีนจะเกิดผลึก 1,3-dinitrobenzene ซึ่งเป็นผลคูณของปฏิกิริยาต่อไปนี้:

ฮาโลเจน หากคุณผสมเบนซินในที่มืดกับคลอรีนหรือโบรมีน มะเร็งจะไม่เกิดขึ้น อย่างไรก็ตาม เมื่อมีตัวเร่งปฏิกิริยาที่มีคุณสมบัติของกรดลิวอิส ปฏิกิริยาการแทนที่ด้วยไฟฟ้าจะเกิดขึ้นในสารผสมดังกล่าว ตัวเร่งปฏิกิริยาทั่วไปสำหรับปฏิกิริยาเหล่านี้ ได้แก่ โบรไมด์เหล็ก (III) และอะลูมิเนียมคลอไรด์ การกระทำของตัวเร่งปฏิกิริยาเหล่านี้คือพวกมันสร้างโพลาไรเซชันในโมเลกุลของฮาโลเจน ซึ่งจะสร้างสารเชิงซ้อนกับตัวเร่งปฏิกิริยา:
แม้ว่าจะไม่มีหลักฐานโดยตรงว่าในกรณีนี้ไอออนอิสระเกิดขึ้น กลไกของโบรมีนเบนซีนโดยใช้โบรไมด์เหล็ก (III) เป็นพาหะไอออนสามารถแสดงได้ดังนี้:

ซัลโฟเนชั่น เบนซีนสามารถถูกทำให้เป็นซัลโฟเนตได้ (แทนที่อะตอมของไฮโดรเจนในนั้นด้วยกลุ่มซัลโฟ) โดยการรีฟลักซ์ของส่วนผสมด้วยกรดซัลฟิวริกเข้มข้นเป็นเวลาหลายชั่วโมง ในทางกลับกัน น้ำมันเบนซินสามารถให้ความร้อนเบา ๆ ผสมกับกรดซัลฟิวริกที่เป็นควันแทนได้ กรดกำมะถันที่เป็นควันประกอบด้วยซัลเฟอร์ไตรออกไซด์ กลไกของปฏิกิริยานี้สามารถแสดงโดยโครงร่าง

ปฏิกิริยาของ Friedel-Crafts ปฏิกิริยาของ Friedel-Crafts เดิมเรียกว่าปฏิกิริยาควบแน่นระหว่างสารประกอบอะโรมาติกและอัลคิลเฮไลด์ในที่ที่มีตัวเร่งปฏิกิริยาอะลูมิเนียมคลอไรด์ปราศจากน้ำ
ในปฏิกิริยาควบแน่น โมเลกุลของสารตั้งต้นสองโมเลกุล (หรือสารตั้งต้นหนึ่งตัว) จะรวมกันเป็นโมเลกุลของสารประกอบใหม่ ในขณะที่โมเลกุลของสารประกอบธรรมดาบางชนิด เช่น น้ำหรือไฮโดรเจนคลอไรด์ จะถูกแยกออกจากพวกมัน .
ในปัจจุบัน ปฏิกิริยาของ Friedel-Crafts เป็นการแทนที่อิเล็กโทรฟิลิกของสารประกอบอะโรมาติกซึ่งคาร์โบเคชั่นหรือสารเชิงซ้อนที่มีโพลาไรซ์สูงที่มีอะตอมของคาร์บอนที่มีประจุบวกทำหน้าที่เป็นอิเล็กโทรไฟล์ สารอิเล็กโตรฟิลลิกมักจะเป็นอัลคิลเฮไลด์หรือคลอไรด์ของกรดคาร์บอกซิลิก แม้ว่าจะยังสามารถเป็นได้ ตัวอย่างเช่น แอลคีนหรือแอลกอฮอล์ อะลูมิเนียมคลอไรด์ปราศจากน้ำมักใช้เป็นตัวเร่งปฏิกิริยาสำหรับปฏิกิริยาเหล่านี้ ปฏิกิริยาของ Friedel-Crafts มักจะแบ่งออกเป็นสองประเภท: alkylation และ acylation
อัลคิเลชั่น ในปฏิกิริยาของ Friedel-Crafts ประเภทนี้ อะตอมไฮโดรเจนหนึ่งอะตอมหรือมากกว่าในวงแหวนเบนซีนจะถูกแทนที่ด้วยหมู่อัลคิล ตัวอย่างเช่น เมื่อส่วนผสมของเบนซีนและคลอโรมีเทนถูกทำให้ร้อนอย่างระมัดระวังในที่ที่มีอะลูมิเนียมคลอไรด์ปราศจากน้ำ เมทิลเบนซีนจะก่อตัวขึ้น คลอโรมีเทนมีบทบาทเป็นตัวแทนอิเล็กโทรฟิลิกในปฏิกิริยานี้ มีโพลาไรซ์โดยอะลูมิเนียมคลอไรด์ในลักษณะเดียวกับที่เกิดขึ้นกับโมเลกุลของฮาโลเจน:
กลไกของปฏิกิริยาที่พิจารณาสามารถแสดงได้ดังนี้:

ควรสังเกตว่าในปฏิกิริยาควบแน่นระหว่างเบนซีนและคลอโรมีเทน โมเลกุลของไฮโดรเจนคลอไรด์จะถูกแยกออก นอกจากนี้เรายังทราบด้วยว่าการมีอยู่จริงของ carbocation ของโลหะในรูปของไอออนอิสระนั้นเป็นที่น่าสงสัย
Alkylation ของเบนซินกับคลอโรมีเทนต่อหน้าตัวเร่งปฏิกิริยา - อะลูมิเนียมคลอไรด์ปราศจากน้ำไม่ได้จบลงด้วยการก่อตัวของเมทิลเบนซีน ในปฏิกิริยานี้ อัลคิเลชันเพิ่มเติมของวงแหวนเบนซีนเกิดขึ้น ซึ่งนำไปสู่การก่อตัวของ 1,2-ไดเมทิลเบนซีน:

อะซิเลชั่น ในปฏิกิริยาของ Friedel-Crafts ประเภทนี้ อะตอมของไฮโดรเจนในวงแหวนเบนซีนจะถูกแทนที่ด้วยกลุ่ม acyl ทำให้เกิดอะโรมาติกคีโตน
หมู่อะซิลมีสูตรทั่วไป
ชื่อที่เป็นระบบของสารประกอบ acyl เกิดขึ้นจากการแทนที่คำต่อท้ายและสิ้นสุด -ova ในชื่อของกรดคาร์บอกซิลิกที่สอดคล้องกัน ซึ่งสารประกอบ acyl ที่ให้มานั้นเป็นอนุพันธ์ โดยมีคำต่อท้าย -(o)yl ตัวอย่างเช่น

Acylation ของเบนซินดำเนินการโดยใช้คลอไรด์หรือแอนไฮไดรด์ของกรดคาร์บอกซิลิกต่อหน้าตัวเร่งปฏิกิริยาอะลูมิเนียมคลอไรด์ที่ปราศจากน้ำ ตัวอย่างเช่น

ปฏิกิริยานี้เป็นการควบแน่นที่เกิดการกำจัดโมเลกุลไฮโดรเจนคลอไรด์ โปรดทราบด้วยว่าชื่อ "ฟีนิล" มักใช้เพื่อระบุวงแหวนเบนซีนในสารประกอบที่เบนซินไม่ใช่กลุ่มหลัก:

ปฏิกิริยาการเติม แม้ว่าน้ำมันเบนซินจะเป็นลักษณะเฉพาะส่วนใหญ่ของปฏิกิริยาการแทนที่อิเล็กโตรฟิลลิก แต่ก็เข้าสู่ปฏิกิริยาการเติมบางส่วนด้วย เราได้พบกับหนึ่งในนั้นแล้ว เรากำลังพูดถึงการเติมไฮโดรเจนของน้ำมันเบนซิน (ดูหัวข้อ 5.3) เมื่อส่วนผสมของเบนซินและไฮโดรเจนถูกส่งผ่านบนพื้นผิวของตัวเร่งปฏิกิริยานิกเกิลแบบละเอียดที่อุณหภูมิ 150–160 °C ปฏิกิริยาทั้งหมดจะเกิดขึ้นตามลำดับ ซึ่งจะจบลงด้วยการก่อตัวของไซโคลเฮกเซน สมการปริมาณสัมพันธ์โดยรวมสำหรับปฏิกิริยานี้สามารถแสดงได้ดังนี้:

ภายใต้อิทธิพลของรังสีอัลตราไวโอเลตหรือแสงแดดโดยตรง เบนซินยังทำปฏิกิริยากับคลอรีน ปฏิกิริยานี้ดำเนินการโดยกลไกหัวรุนแรงที่ซับซ้อน ผลิตภัณฑ์ขั้นสุดท้ายคือ 1,2,3,4,5,6-เฮกซะคลอโรไซโคลเฮกเซน:

ปฏิกิริยาที่คล้ายกันเกิดขึ้นระหว่างเบนซีนและโบรมีนภายใต้การกระทำของรังสีอัลตราไวโอเลตหรือแสงแดด
ออกซิเดชัน. เบนซีนและวงแหวนเบนซีนในสารประกอบอะโรมาติกอื่นๆ โดยทั่วไปจะทนต่อการเกิดออกซิเดชันได้ แม้กระทั่งโดยตัวออกซิไดซ์ที่แรงเช่น สารละลายที่เป็นกรดหรือด่างของโพแทสเซียม เปอร์แมงกาเนต อย่างไรก็ตาม น้ำมันเบนซินและอะโรเมติกส์อื่นๆ เผาไหม้ในอากาศหรือออกซิเจนเพื่อสร้างเปลวไฟที่มีควันมาก ซึ่งเป็นลักษณะของไฮโดรคาร์บอนที่มีปริมาณคาร์บอนสัมพัทธ์สูง

คุณสมบัติทางกายภาพ
น้ำมันเบนซินและสารที่คล้ายคลึงกันที่ใกล้เคียงที่สุดคือของเหลวไม่มีสีมีกลิ่นเฉพาะ อะโรมาติกไฮโดรคาร์บอนมีน้ำหนักเบากว่าน้ำและไม่ละลายในนั้น แต่ละลายได้ง่ายในตัวทำละลายอินทรีย์ - แอลกอฮอล์ อีเธอร์ อะซิโตน
เบนซีนและสารคล้ายคลึงกันเป็นตัวทำละลายที่ดีสำหรับสารอินทรีย์หลายชนิด เวทีทั้งหมดเผาไหม้ด้วยเปลวไฟที่มีควันเนื่องจากมีปริมาณคาร์บอนสูงของโมเลกุล
คุณสมบัติทางกายภาพของบาง arenes แสดงไว้ในตาราง
ตาราง. คุณสมบัติทางกายภาพของบางเวที
|
ชื่อ |
สูตร |
t°.pl., |
t°.bp., |
|
เบนซิน |
C 6 H 6 |
5,5 |
80,1 |
|
โทลูอีน (เมทิลเบนซีน) |
C 6 H 5 CH 3 |
95,0 |
110,6 |
|
เอทิลเบนซีน |
C 6 H 5 C 2 H 5 |
95,0 |
136,2 |
|
ไซลีน (ไดเมทิลเบนซีน) |
C 6 H 4 (CH 3) 2 |
||
|
ออร์โธ- |
25,18 |
144,41 |
|
|
เมตา- |
47,87 |
139,10 |
|
|
คู่- |
13,26 |
138,35 |
|
|
โพรพิลเบนซีน |
C 6 H 5 (CH 2) 2 CH 3 |
99,0 |
159,20 |
|
คิวมีน (ไอโซโพรพิลเบนซีน) |
C 6 H 5 CH(CH 3) 2 |
96,0 |
152,39 |
|
สไตรีน (ไวนิลเบนซีน) |
C 6 H 5 CH \u003d CH 2 |
30,6 |
145,2 |
เบนซิน - เดือดต่ำ ( tkip= 80.1°C) ของเหลวไม่มีสี ไม่ละลายในน้ำ
ความสนใจ! เบนซิน - พิษ ออกฤทธิ์ต่อไต เปลี่ยนสูตรเลือด (เมื่อสัมผัสเป็นเวลานาน) สามารถทำลายโครงสร้างของโครโมโซมได้
อะโรมาติกไฮโดรคาร์บอนส่วนใหญ่เป็นอันตรายถึงชีวิตและเป็นพิษ
ได้รับ arenes (เบนซินและคล้ายคลึงกัน)
ในห้องปฏิบัติการ
1. การรวมตัวของเกลือของกรดเบนโซอิกกับด่างที่เป็นของแข็ง
C 6 H 5 -COONa + NaOH เสื้อ → C 6 H 6 + Na 2 CO 3
โซเดียมเบนโซเอต
2. ปฏิกิริยาของ Wurtz-Fitting: (ที่นี่ G คือฮาโลเจน)
ตั้งแต่6ชม 5 -G+2นา + R-G →ค 6 ชม 5 - R + 2 นาจี
กับ 6 H 5 -Cl + 2Na + CH 3 -Cl → C 6 H 5 -CH 3 + 2NaCl
ในอุตสาหกรรม
- แยกได้จากน้ำมันและถ่านหินโดยการกลั่นแบบเศษส่วน ปฏิรูป;
- จากน้ำมันถ่านหินและแก๊สเตาอบโค้ก
1. ดีไฮโดรไซไลเซชันของอัลเคนด้วยอะตอมของคาร์บอนมากกว่า 6 อะตอม:
C 6 H 14 t , kat→C 6 H 6 + 4H 2
2. ทริมเมอไรเซชันของอะเซทิลีน(สำหรับเบนซินเท่านั้น) – ร. เซลินสกี้:
3C 2 H2 600 °ค, กระทำ. ถ่านหิน→C 6 H 6
3. ดีไฮโดรจีเนชันไซโคลเฮกเซนและคล้ายคลึงกัน:
นักวิชาการโซเวียต นิโคไล ดมิตรีเยวิช เซลินสกี้ ยอมรับว่าน้ำมันเบนซินเกิดจากไซโคลเฮกเซน (ดีไฮโดรจีเนชันของไซโคลอัลเคน
C 6 H 12 ที แมว→C 6 H 6 + 3H 2

C 6 H 11 -CH 3 t , kat→C 6 H 5 -CH 3 + 3H 2
เมทิลไซโคลเฮกเซนโทลูอีน
4. Alkylation ของเบนซิน(ได้รับสารคล้ายคลึงกันของเบนซิน) – อาร์ ฟรีเดล-คราฟต์.
C 6 H 6 + C 2 H 5 -Cl t, AlCl3→C 6 H 5 -C 2 H 5 + HCl
คลอโรอีเทน เอทิลเบนซีน

คุณสมบัติทางเคมีของ arenes
ฉัน. ปฏิกิริยาออกซิเดชัน
1. การเผาไหม้ (เปลวไฟควัน):
2C 6 H 6 + 15O 2 t→12CO 2 + 6H 2 O + Q
2. ภายใต้สภาวะปกติ เบนซินจะไม่ทำให้น้ำโบรมีนเปลี่ยนสีและสารละลายโพแทสเซียมเปอร์แมงกาเนตที่เป็นน้ำ
3. สารคล้ายคลึงเบนซีนถูกออกซิไดซ์โดยโพแทสเซียมเปอร์แมงกาเนต (โพแทสเซียมเปอร์แมงกาเนตเปลี่ยนสี):
ก) ในสภาพแวดล้อมที่เป็นกรดถึงกรดเบนโซอิก
ภายใต้การกระทำของโพแทสเซียมเปอร์แมงกาเนตและสารออกซิไดซ์ที่แรงอื่น ๆ ในสารคล้ายคลึงกันของเบนซีนโซ่ด้านข้างจะถูกออกซิไดซ์ ไม่ว่าสายโซ่ของสารทดแทนจะซับซ้อนแค่ไหน มันก็ถูกทำลาย ยกเว้นอะตอม a -คาร์บอน ซึ่งถูกออกซิไดซ์เป็นกลุ่มคาร์บอกซิล
ความคล้ายคลึงกันของน้ำมันเบนซินที่มีสายโซ่ด้านเดียวให้กรดเบนโซอิก:
คล้ายคลึงกันที่มีโซ่สองข้างให้กรดไดเบสิก:
5C 6 H 5 -C 2 H 5 + 12KMnO 4 + 18H 2 SO 4 → 5C 6 H 5 COOH + 5CO 2 + 6K 2 SO 4 + 12MnSO 4 + 28H 2 O
5C 6 H 5 -CH 3 + 6KMnO 4 + 9H 2 SO 4 → 5C 6 H 5 COOH + 3K 2 SO 4 + 6MnSO 4 + 14H 2 O
ตัวย่อ :
C 6 H 5 -CH 3 + 3O KMnO4→C 6 H 5 COOH + H 2 O
B) เป็นกลางและเป็นด่างเล็กน้อยถึงเกลือของกรดเบนโซอิก
C 6 H 5 -CH 3 + 2KMnO 4 → C 6 H 5 COO K + K OH + 2MnO 2 + H 2 O
II. ปฏิกิริยาเพิ่มเติม (แข็งกว่าแอลคีน)
1. ฮาโลเจน
C 6 H 6 + 3Cl 2 ชม. ν → C 6 H 6 Cl 6 (เฮกซาคลอโรไซโคลเฮกเซน - เฮกซาคลอแรน)
2. ไฮโดรจีเนชัน
C 6 H 6 + 3H 2 t , ปตทหรือนิ→C 6 H 12 (ไซโคลเฮกเซน)
3. พอลิเมอไรเซชัน
สาม. ปฏิกิริยาการทดแทน – กลไกไอออนิก (เบากว่าอัลเคน)
b) น้ำมันเบนซินคล้ายคลึงกันเมื่อฉายรังสีหรือให้ความร้อน
ในแง่ของคุณสมบัติทางเคมี อัลคิลเรดิคัลมีความคล้ายคลึงกับอัลเคน อะตอมไฮโดรเจนในพวกมันถูกแทนที่ด้วยฮาโลเจนด้วยกลไกของอนุมูลอิสระ ดังนั้น ในกรณีที่ไม่มีตัวเร่งปฏิกิริยา การให้ความร้อนหรือการฉายรังสี UV จะนำไปสู่ปฏิกิริยาการแทนที่ที่รุนแรงในสายด้านข้าง อิทธิพลของวงแหวนเบนซีนที่มีต่อหมู่แทนที่อัลคิลนำไปสู่ความจริงที่ว่า อะตอมของไฮโดรเจนจะถูกแทนที่เสมอที่อะตอมของคาร์บอนที่ผูกมัดโดยตรงกับวงแหวนเบนซีน (อะตอมของคาร์บอน)
1) C 6 H 5 -CH 3 + Cl 2 ชม. ν → C 6 H 5 -CH 2 -Cl + HCl
c) homologues เบนซินต่อหน้าตัวเร่งปฏิกิริยา
C 6 H 5 -CH 3 + Cl 2 AlCl 3 → (ส่วนผสมของออร์ตา, คู่ของอนุพันธ์) +HCl
2. ไนเตรชั่น (ด้วยกรดไนตริก)
C 6 H 6 + HO-NO 2 t, H2SO4→C 6 H 5 -NO 2 + H 2 O
ไนโตรเบนซีน - กลิ่น อัลมอนด์!
C 6 H 5 -CH 3 + 3HO-NO 2 t, H2SO4→ กับ H 3 -C 6 H 2 (NO 2) 3 + 3H 2 O2,4,6-ไตรไนโตรโทลูอีน (ทอล, ทรอทิล)
การใช้น้ำมันเบนซินและสารคล้ายคลึงกัน
เบนซิน C 6 H 6 เป็นตัวทำละลายที่ดี น้ำมันเบนซินเป็นสารเติมแต่งช่วยเพิ่มคุณภาพของเชื้อเพลิงเครื่องยนต์ ทำหน้าที่เป็นวัตถุดิบสำหรับการผลิตสารประกอบอินทรีย์อะโรมาติกหลายชนิด - ไนโตรเบนซีน C 6 H 5 NO 2 (ได้ตัวทำละลาย aniline มาจากมัน) คลอโรเบนซีน C 6 H 5 Cl ฟีนอล C 6 H 5 OH สไตรีน ฯลฯ
โทลูอีน C 6 H 5 -CH 3 - ตัวทำละลายที่ใช้ในการผลิตสีย้อม ยาและวัตถุระเบิด (trotyl (tol) หรือ 2,4,6-trinitrotoluene TNT)
ไซลีนค 6 H 4 (CH 3) 2 . เทคนิคไซลีนเป็นส่วนผสมของไอโซเมอร์สามตัว ( ortho-, เมต้า- และ คู่-ไซลีน) - ใช้เป็นตัวทำละลายและผลิตภัณฑ์เริ่มต้นสำหรับการสังเคราะห์สารประกอบอินทรีย์หลายชนิด
ไอโซโพรพิลเบนซีน C 6 H 5 -CH (CH 3) 2 ทำหน้าที่เพื่อให้ได้ฟีนอลและอะซิโตน
อนุพันธ์คลอรีนของเบนซีนใช้สำหรับป้องกันพืช ดังนั้นผลคูณของการแทนที่ของอะตอม H ในเบนซีนด้วยอะตอมของคลอรีนคือเฮกซาคลอโรเบนซีน C 6 Cl 6 - ยาฆ่าเชื้อรา ใช้สำหรับแต่งเมล็ดข้าวสาลีและข้าวไรย์กับเมล็ดแห้งที่มีคราบเขม่าแข็ง ผลิตภัณฑ์จากการเติมคลอรีนลงในเบนซีนคือเฮกซาคลอโรไซโคลเฮกเซน (เฮกซาคลอแรน) C 6 H 6 Cl 6 - ยาฆ่าแมลง มันถูกใช้เพื่อควบคุมแมลงที่เป็นอันตราย สารเหล่านี้หมายถึงยาฆ่าแมลง - วิธีการทางเคมีในการต่อสู้กับจุลินทรีย์ พืช และสัตว์
สไตรีน C 6 H 5 - CH \u003d CH 2 โพลิเมอไรเซชันได้ง่ายมาก ขึ้นรูปเป็นพอลิสไตรีน และโคพอลิเมอไรเซชันกับยางบิวทาไดอีน - สไตรีน-บิวทาไดอีน
ประสบการณ์วิดีโอ
